唾液中の細菌と認知機能との相関をAIで診断
唾液細菌叢は、バイオマーカーとしてどのような可能性を秘めているのか。先行研究によれば、次のような疾患との関連が明らかになっている。
口腔がん・肥満・肺炎・IgA腎症・肝硬変・関節リウマチ・原発性硬化性胆管炎・潰瘍性大腸炎・膵臓がんなどとの関連性だ。これを見ればわかるように、これまでのところ認知症につながる神経変性疾患との関連は明らかになっていない。
「それでも新しい手法を取り込めば、神経変性疾患を見分ける可能性が出てくるのではないかと考えました。私たちはこれを生理的変動マーカーと位置付けており、従来のバイオマーカーとは異なります」
「これまでのバイオマーカーでは、マーカーとなる特定のタンパク質や核酸と疾患が1対1の対応関係となっていました。たとえばアルツハイマー病のバイオマーカーのひとつとして知られているアミロイドβや、前立腺がんのPSA(Prostate-specific antigen)などです。これらのタンパク質が血液などの生体試料中に存在しているか、存在していればどの程度かによって病気の有無を見分けます」
「生理的変動マーカーでは、マーカーと疾患の関係性を、このような1対1の関係性として捉えません。マーカーとしてたとえば唾液中の80種類の菌の発現パターンをチェックし、それらの変動状態をもとに複数の疾患を同時に見極めるのです」
次世代シークエンサーにより、唾液に含まれる細菌の種類やその存在比率を網羅的に調べられる。その中から特定の菌の存在量を機械学習にかけて、複数の疾患を見極める。マーカーと疾患を1対1対応で判断する通常のバイオマーカーとは、根本的にコンセプトの異なる解析手法である。
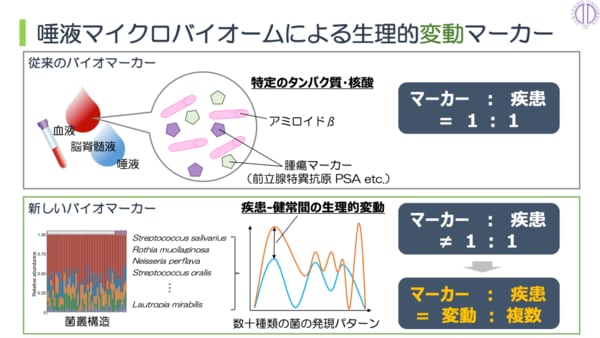 スライド:久松氏提供
スライド:久松氏提供
「生理的変動マーカーにより明らかになったのが、唾液マイクロバイオームが持つ神経変性疾患のバイオマーカーとしての可能性です。唾液細菌は腸内細菌よりも特定の神経変性疾患を高精度に見極められることがわかりました」
「その結果、認知症の進行度を判断できたり、将来パーキンソン病などになる可能性が高いとされているレム睡眠行動異常症など、いわゆる前駆症状を早期に判別できたりするようになります。具体的にはアルツハイマー病、レビー小体型認知症、さらにパーキンソン病など、異常なタンパク質の蓄積を原因とする神経変性疾患を見極められるのです。さらに特定の薬によっても唾液マイクロバイオームが変化することがわかり、治療薬の影響も評価できる可能性があります」
久松氏の研究成果『神経変性疾患のリスク判定方法及び装置』については、国内特許取得の後に指定国(米国・欧州・韓国・カタール)での特許査定移行申請も行われている。ほかにも複数の特許を取得済みだ。
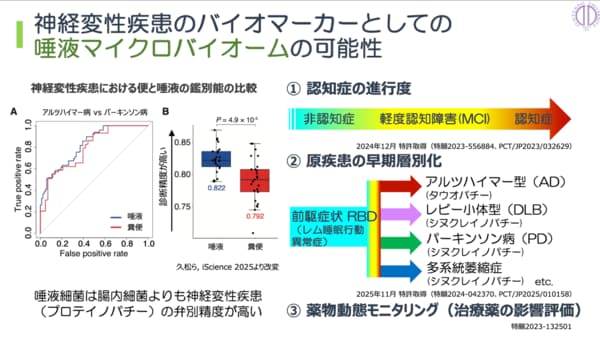 スライド:久松氏提供
スライド:久松氏提供