ゲノム編集が大きく前進するかもしれない(写真:Natali _ Mis/Shutterstock.com)
ゲノム編集が大きく前進するかもしれない(写真:Natali _ Mis/Shutterstock.com)
既存の学問領域にとらわれない研究を推進するフォーラム「Scienc-ome」に集う研究者が未来を語る連載。第3回では、画期的な技術開発によりアメリカで起業したバイオベンチャー、One Genomics(ワン・ゲノミクス)を紹介する。
ノーベル賞を受賞しながらも精度に問題があるため、今ひとつ実用化につながっていなかったゲノム編集技術「CRISPR-Cas9(クリスパー・キャス9)」。そのゲノム編集の精度を格段に高める「セイフガードgRNA」を、九州大学生体防御医学研究所の川又理樹助教が開発した。川又氏は、マサチューセッツ工科大学(MIT)でMBA取得後にメタ(旧フェイスブック)で事業推進を担当したダイアナ・ラン氏、連載第1回で紹介した慶應義塾大学の早野元詞氏と3人でOne Genomicsを起業。舞台は日本ではなくあえてアメリカを選択した。背景にあるのは、市場環境を冷静に見すえた企業戦略である。
(竹林 篤実:理系ライターズ「チーム・パスカル」代表)
「Scienc-ome」とは
新進気鋭の研究者たちが、オンラインで最新の研究成果を発表し合って交流するフォーラム。「反分野的」をキャッチフレーズに、既存の学問領域にとらわれない、ボーダーレスな研究とイノベーションの推進に力を入れている。フォーラムは基本的に毎週水曜日21時~22時(日本時間)に開催され、アメリカ、ヨーロッパ、中国など世界中から参加ができる。企業や投資家、さらに高校生も参加している。>>フォーラムへ
ゲノム編集の精度と安全性を100倍以上に向上
2020年のノーベル化学賞は、微生物学者のエマニュエル・シャルパンティエ教授と生化学者のジェニファー・ダウドナ教授に贈られた。対象となったのは、2人によって開発されたゲノム編集技術「CRISPR-Cas9」である。ゲノム編集の革新的技術と評価されたCRISPR-Cas9だが、医療分野での応用は当初期待されたほど進んでいない。その理由は、狙ったところ以外のDNAまでを切断してしまうリスクなどにある。九州大学生体防御医学研究所の川又理樹助教が解説する。
 ゲノム編集技術「CRISPR-Cas9(クリスパー・キャス9)」で2020年のノーベル化学賞を受賞した、微生物学者のエマニュエル・シャルパンティエ教授(左)と生化学者のジェニファー・ダウドナ教授(右)(写真:Agencia EFE/アフロ)
ゲノム編集技術「CRISPR-Cas9(クリスパー・キャス9)」で2020年のノーベル化学賞を受賞した、微生物学者のエマニュエル・シャルパンティエ教授(左)と生化学者のジェニファー・ダウドナ教授(右)(写真:Agencia EFE/アフロ)
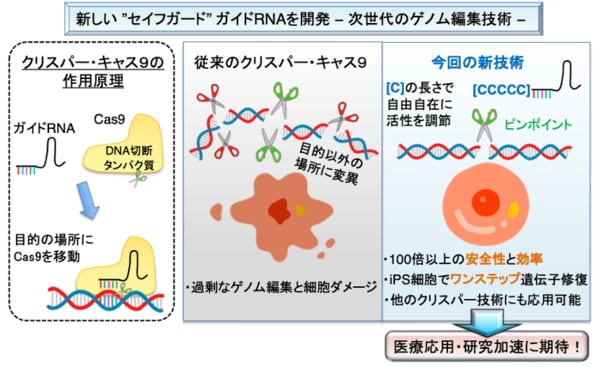
「CRISPR-Cas9とは、DNAを切断する酵素Cas9と、Cas9をDNAの特定の部分に導くガイドgRNAを組み合わせた技術です。ただCas9の切断活性が非常に強いために、たとえば目的とする場所以外のDNAを切断したり、狙っているのが父型由来の染色体上のDNAなのに、母型由来の染色体上の同じ部分にまで作用してしまったりといった問題がありました」
問題は過剰な切断活性にあり、活性をいかに抑制するかが課題となっていた。この課題を解消するため、川又氏らによって開発された革新的な技術が「セイフガードgRNA」である。
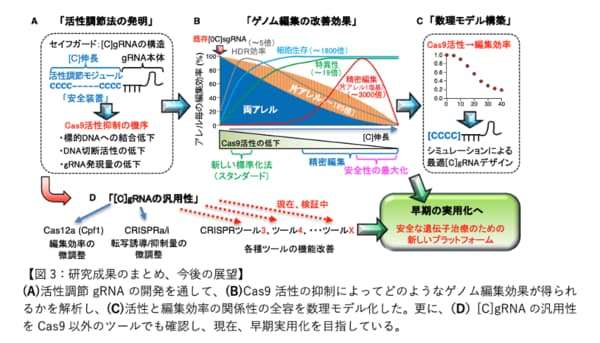
「CRISPR-Cas9の活性を下げるためには、どうすればよいか。試行錯誤した末に発見したのが、gRNAにシトシン塩基(C)を付加するアイデアでした。しかも付け加えるCの長さにより、Cas9の活性を自由自在にコントロールできるとわかったのです。その結果、狙った場所だけを切断する正確さが、単にCRISPR-Cas9だけを使う場合の19倍まで高まり、安全性や精密さは100倍以上と飛躍的な改善を実現できました」
 川又 理樹(かわまた・まさき) 九州大学生体防御医学研究所助教
川又 理樹(かわまた・まさき) 九州大学生体防御医学研究所助教1979年、栃木県真岡市生まれ。2007年、東北大学農学研究科博士課程修了、博士(農学)。2007年より国立がん研究センターリサーチレジデント、2013年よりハーバード大学Fernando Camargo博士のラボに所属し、ボストン小児病院、ハーバード幹細胞研究所にてResearch Fellow。2016年より現職。2023年2月25日に、九州大学から出願した新規CRISPR-Cas9ゲノム編集法に関する特許をもとに、アメリカでOne Genomics, Inc.を起業。
切断の精度などCRISPR-Cas9を医療応用するために解消すべき課題は、この技術が発明された2012年以来ずっと、世界中の研究者に認識されていた。けれども、課題解決の決定打となるgRNAによる微調節技術は川又氏の研究以前には出ていない。川又氏らは研究成果を社会実装するために、日本はもとよりアメリカ、ヨーロッパ、中国などで特許を出願した。そのうえでバイオベンチャー、One Genomicsを、日本ではなくあえてアメリカで起業した。