再生医療によるがん治療、いわゆる遺伝子細胞治療に代表される技術は、驚くべきスピードで進歩している。国による法整備や予算の拡大に加えて、再生医療の研究開発から製造、商業化までを見据えたソリューションが相次いで登場し、細胞やウイルスなどを用いた製剤の開発が加速しているからだ。再生医療によるがん治療の現状と今後について、ライフサイエンス業界のグローバル・リーディングカンパニー、サーモフィッシャーサイエンティフィック(以下、サーモフィッシャー)に伺った。
完全寛解の可能性もある再生医療によるがん治療
これまでのがん治療と再生医療によるがん治療の大きな違いは、がん細胞を狙って治療することができるかどうかである。再生医療では、細胞やウイルスが有する機能を利用し、それらにがん細胞を認識させ、攻撃させる。
かつてのがんの三大治療といえば、外科的な手術療法、抗がん剤を用いた薬物療法、そして放射線療法で、これらはがんの進行を抑えるのが精いっぱいだった。一方、近年では抗体などのバイオ医薬品の普及により、がん治療に大きなブレークスルーを与えてきたが、さらに再生医療によるがん治療では、難治性のがんに対する可能性も見えてきたという。
世界的に見て、再生医療によるがん治療は血液がんの領域で実績が多い。白血病は血液細胞を作りだす元となる細胞ががん化する病気だ。そのがん細胞は自己増殖し、血液中に流れていくので、放射線を当てたり、薬物を投与しても、その効果は一過性で、患者への負担が大きかった。しかし、「CAR-T細胞療法」(※詳細は後述)によって、骨髄移植を待っているような小児がん患者が完全寛解した事例が報告された。
再生医療に用いる細胞やウイルス由来の製剤の開発には、3つのプレーヤーが関わっている。1つ目は、シーズ開発を担うアカデミア(大学の研究室、公的研究機関)。2つ目は、シーズを基にビジネス展開を図る創薬型のバイオベンチャー企業。そして3つ目が、実際に製造・販売する製薬会社や製造開発を支援するCDMO(Contract Development and Manufacturing Organization)だ。サーモフィッシャーでは、3つのプレーヤーそれぞれに幅広いソリューションを提供している。
「アカデミアやバイオベンチャー企業に対しては研究開発に必要な研究用試薬や装置を、製薬会社やCDMOには製造用の装置や資材、製造支援サービスなどを提供しています。近年では研究開発から製造まで一貫して使用できる規制面を考慮した原材料のラインアップの拡充に努めています。また、グループ内にCDMO(医薬品の開発・製造受託)機能を拡大し、バイオテック企業や医薬品メーカーの製造・開発をより幅広くサポートできるようになりました」。アカデミアとのビジネスを手がけるバイオサイエンス ビジネスデベロップメントマネージャー 荻田 伸夫氏はこう説明する。
コストと時間が細胞製剤の大きな課題
先述のCAR-T細胞を例に、製剤の製品化までにどのようなプロセスがあり、またどのような課題があるのかを紹介したい。
まず、①血液がんの患者から血液を採取し、凍結して製造工場に送る。②届いた血液を融解し、目的の細胞となるT細胞(免疫細胞の一種)を分離する。③分離したT細胞に外から遺伝子を導入し、がん細胞を認識する機能を持たせる。④それがCAR-T細胞であり、必要数まで増殖させて増やしていく。⑤増やしたCAR-T細胞は洗浄後、凍結保存して病院へ輸送される。それを病院で解凍し、製剤化した上で患者に投与する――。大まかに言うと、こうだ。
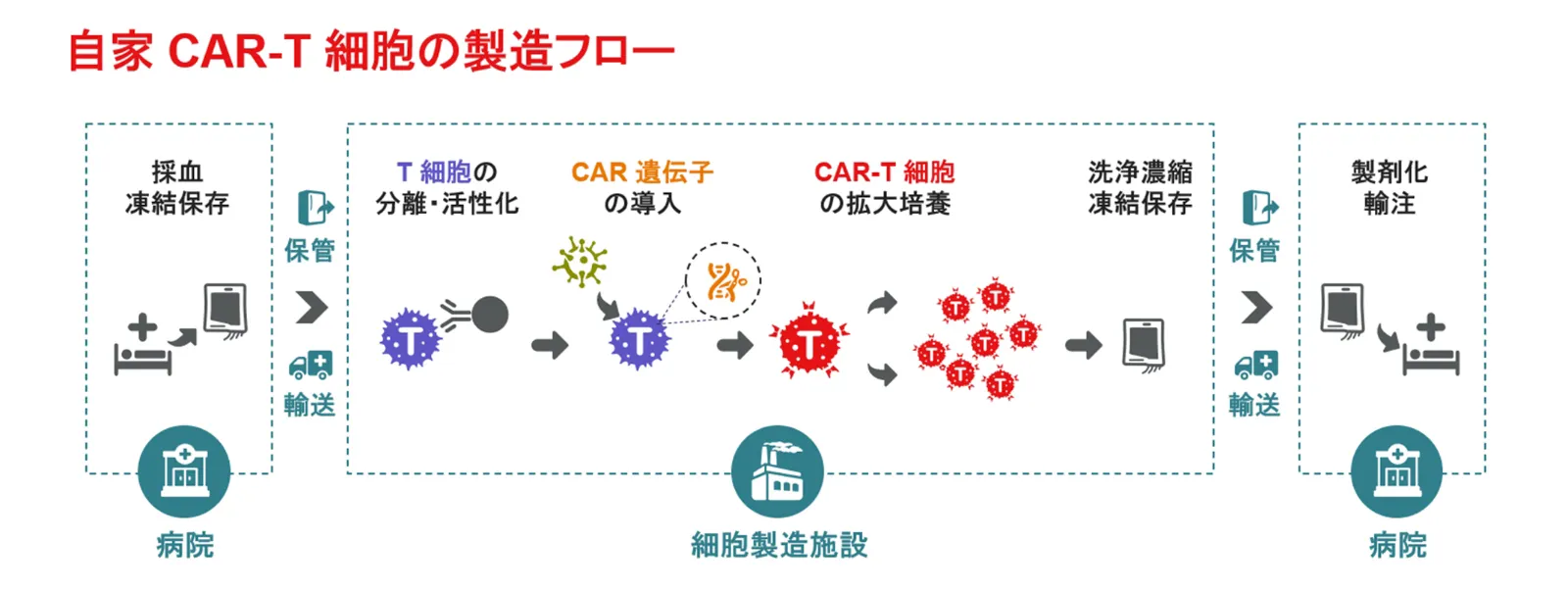
では課題は何か?「ひとえに人手による作業が多くて、煩雑なことです。その結果、コストや時間が非常にかかります」と荻田氏は言う。そもそもの製造方法が、アカデミアの研究室で行われていた“実験操作の域”を出ていないことから課題が多く、コストも膨らむ。1治療あたりの薬価は数千万を超えることが取り沙汰されるが、一方でこれらの治療法が患者へもたらすメリットも大きく、両サイドの視点から活発に論じられるべきである。時間についても、血液を採取してから患者に戻すまでに約2週間、海外の工場に輸送して製造するとなると往復で1カ月程度かかる。末期症状の患者にとっては待ったなしの状況であるため、製造に携わる現場では強い使命感と責任感をもって実施されている。
こうした課題の解決に向けて、サーモフィッシャーでは、アカデミアに対してシーズ開発の段階から商業化の出口を見据えた、品質の高い原材料や製造方法などを提供することで、製品開発の加速につなげている。

製造装置を扱うバイオプロダクション フィールドアプリケーションサイエンティスト 鳥海 健太郎氏は次のように話す。「手作業によるところが多かった製造プロセスを自動化することも、われわれは提案しています。当社のコンセプトは全製造工程を全自動で行うのではなく、複数の自動化装置を組み合わせたモジュール型の製造方法を活用するものです。これによって、各工程をファインチューンして製造工程全体の生産性を高めることが期待でき、また製造サイトの設備コストを低減することにつながると考えています」。
バイオテックや製薬会社にとっては、CDMOを活用することは商業化を加速させる有力な選択肢となるだろう。「ベンチャーはリソースを選択、集中することで開発を進めていらっしゃいます。大手製薬会社にとっても再生細胞医療は新しい分野であるため、設備やノウハウなどの部分においてもパートナーと組んで開発するケースも多く出てきました。われわれはそのようなパートナーの一社となるよう、医薬品の開発・製造の受託サービスを提供しています」。サーモフィッシャーでCDMO事業に携わるファーマサービシズのシニアダイレクター 谷元 浩二氏はこう話す。
サーモフィッシャーのファーマサービシズビジネスはCDMOとして20年を超える実績を持ち、CAR-T細胞やウイルスベクター(遺伝子を改変したウイルス)、コロナワクチンでも知られるメッセンジャーRNA(mRNA)などの製造を手がけている。開発・製造だけでなく、超低温輸送などの高い要件が求められるロジスティクスについてもサポートしているのが特長だ。
研究開発と商業化の“橋渡し”を務めたい
再生医療によるがん治療の進展をグローバルで比較すると、やはり先行しているのは欧米であり、日本は遅れていると言わざるを得ない。今日現在、欧米ではすでに7製品の製剤が上市されており、上市に近い治験中の製剤も多い。一方で、日本では近年承認数が増えてはいるものの上市されているのは4製品にとどまる。このうち日本発の製剤は1製品で、残りは海外からの導入品となっている。
「国内で再生医療によるがん治療の医薬品が承認されたのは、ここ数年の話です。国内でCAR-T製剤が承認されたことをきっかけに、またさらに患者さんへの周知が進んでいくことで、国内の市場も巻き返してスピードが加速し、治療事例も増えていくのではないでしょうか。普段お話しをさせていただくCDMOや製薬企業、ベンチャーそしてアカデミアの皆さま、いずれも本気で薬を世の中に届けたいという強い使命を持って取り組まれていることを感じます」と鳥海氏は期待を寄せる。
再生治療によるがん治療の未来に向けて、“橋渡し”を務めたいと荻田氏は力を込める。「研究開発と商業化の橋渡しにより、より多くの研究成果をより早く社会に送り出していくことが、ライフサイエンス業界のリーディングカンパニーであるわれわれの使命であると考えています」(荻田氏)。
幅広い製品ラインナップとコンサルティングサービス、米国をはじめ海外に数多くの拠点を持ち、グローバルなトレンドを見ながら、最新のライフサイエンスのテクノロジーやソリューションを提案できる競争優位を活かし、日本国内の再生医療とがん治療のプレーヤーをサポートしていく方針だ。
サーモフィッシャーの取り組みによって、シーズ開発の出発点から商業化のゴールまでの時間を短縮することができれば、コスト削減にもつながり、再生医療によるがん治療はより身近な治療になるだろう。また、治療の対象として、現在は白血病などの血液がんが主流だが、今後は固形がんへの適応も期待されている。実際、世界ではさまざまな固形がんを対象とした製剤の治験がスタートしており、国内でも開発が進む。その実現はまだ先だが、がん患者の方々がこの画期的な治療を一日でも早く望まれることも事実。研究開発から商業化への「橋渡し」を担う役割は今後ますます大きくなるだろう。